Heb je hier wat aan gehad? Abonneer dan op mijn YouTube kanaal: ![]()
Doneer meneer Wietsma een kopje koffie: ![]()
Klik hier voor een samenvatting van de video
Vast
– Heeft zijn eigen vorm (niet vervormbaar)
– Moleculen zitten op vaste plek
– Heeft constant volume

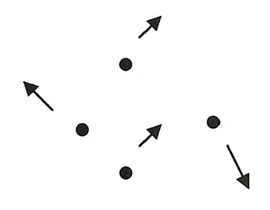
Vloeibaar
– Heeft geen eigen vorm (vervormbaar)
– Moleculen zitten niet vaste plek maar blijven bij elkaar
– Heeft constant volume
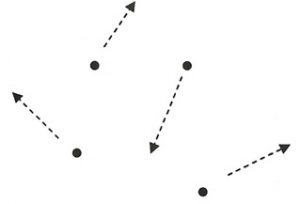
Gas
– Heeft geen eigen vorm (vervormbaar)
– Moleculen zitten niet op vaste plek en blijven niet bij elkaar
– Heeft geen constant volume
Wanneer een stof van de ene naar de andere fase gaat noemen we dit een faseovergang. Hieronder zie je alle faseovergangen
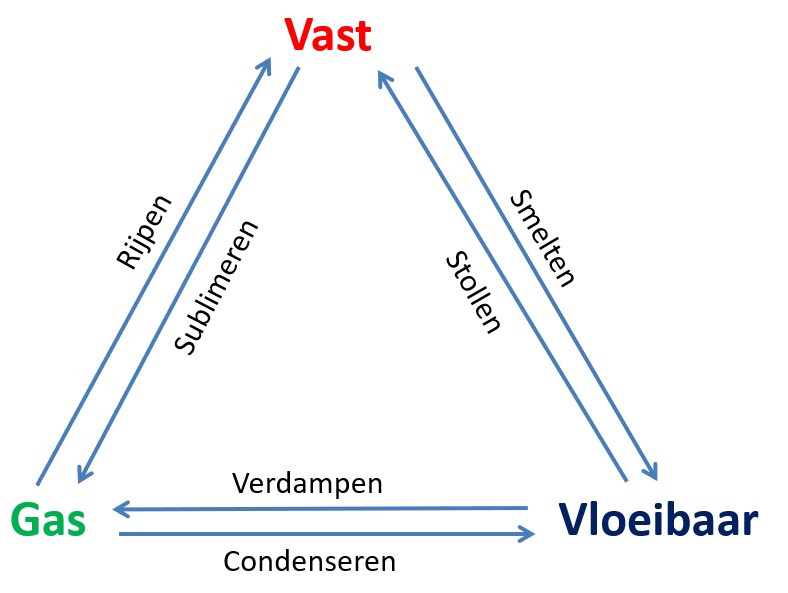
LET OP: Bevriezen en ontdooien staan hier niet tussen en gebruiken we liever niet. Als water vast wordt dan kunnen we zeggen dat het stolt of bevriest, maar als kaarsvet vast wordt, stolt het alleen (het bevriest niet), dus stollen kun je altijd gebruiken en is dus een betere term.
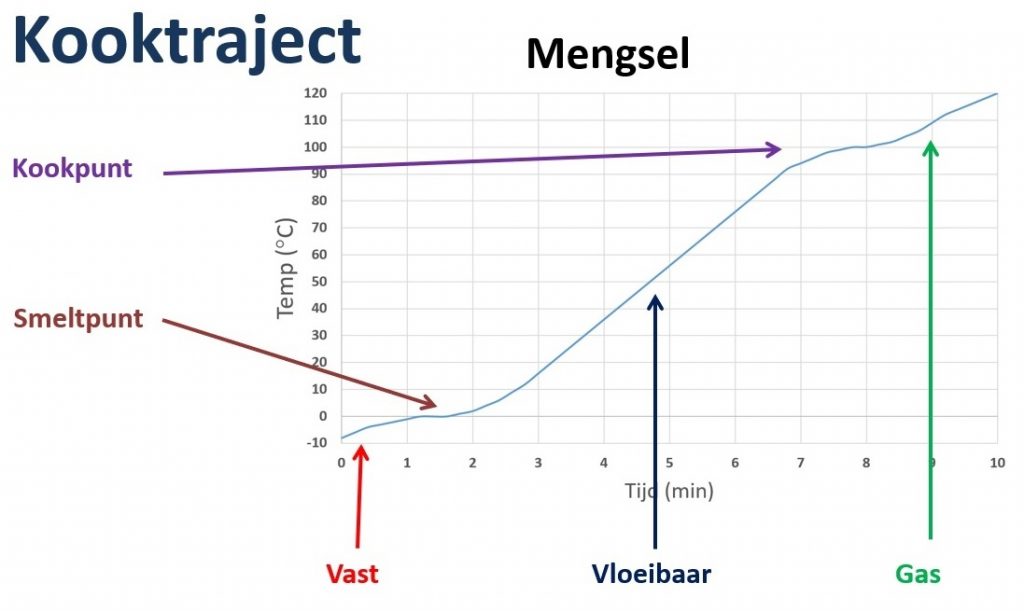
Wanneer we ijs op een warmtebron zetten zal de temperatuur stijgen. In de onderste grafiek zie je hoe dit in de tijd verloopt.
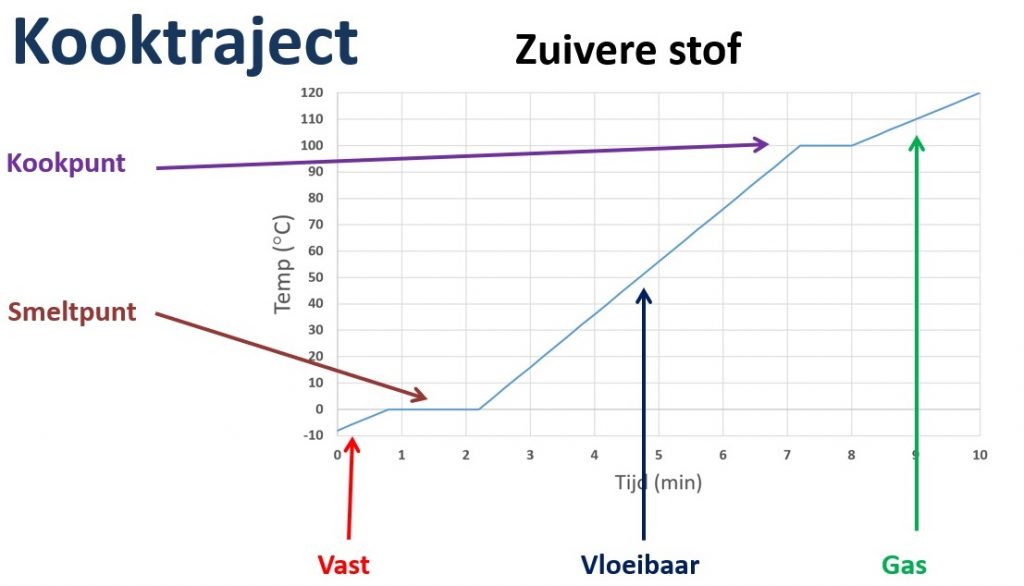
Je ziet twee punten waarbij de temperatuur even stopt met stijgen. Op deze punten is een faseovergang bezit. Op het moment dat de faseovergang plaats vindt zal de temperatuur niet veranderen. De eerste faseovergang bij 0°C is bij water het smeltpunt. Daarna hebben we weer een faseovergang bij 100 °C, dit noemen we het kookpunt.
Bij een zuivere stof zijn deze punten goed te zien en rechte lijnen. Bij een mengsel hebben we meerdere stoffen die ieder een eigen smeltpunt en kookpunt hebben. Er is dus geen spraken meer van een mooie rechte lijn.
Quiz-summary
0 of 8 questions completed
Questions:
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
Information
Maak de quiz om te zien of je het snapt
You have already completed the quiz before. Hence you can not start it again.
Quiz is loading...
You must sign in or sign up to start the quiz.
You have to finish following quiz, to start this quiz:
Resultaten
0 van de 8 vragen goed
Time has elapsed
Categories
- Not categorized 0%
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- Beantwoord
-
Vraag 1 van 8
1. Question
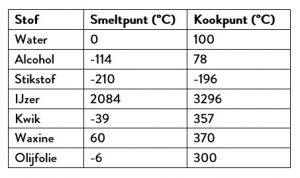
Het is 20 °C. Welke stoffen zijn in vloeibare fase?
 Correct
Correct
Incorrect
-
Vraag 2 van 8
2. Question
Het is -1 °C. Welke stoffen zijn in vaste fase?
 Correct
Correct
Incorrect
-
Vraag 3 van 8
3. Question
Het is 350 °C. Welke stoffen zijn in gasfase?
 Correct
Correct
Incorrect
-
Vraag 4 van 8
4. Question
Je legt boter op een hete pan. Welke faseovergang vindt er plaats?
Correct
Incorrect
-
Vraag 5 van 8
5. Question
Tijdens het douchen beslaat de spiegel. Welke faseovergang vindt er plaats op de spiegel?
Correct
Incorrect
-
Vraag 6 van 8
6. Question
Na een paar warme dagen daalt de waterspiegel in een meer. Welke faseovergang vindt er plaats?
Correct
Incorrect
-
Vraag 7 van 8
7. Question
Je blaast een kaars uit. Het vloeibare kaarsvet gaat nu?
Correct
Incorrect
-
Vraag 8 van 8
8. Question
Uit het niks ontstaan er ijskristalen op het gras. Welke faseovergang vindt er plaats?
Correct
Incorrect


Laat een bericht achter
19 berichten op "Faseovergangen en kooktraject"
bedankt voor de hulp! u gaat naar de HEMEL!!!!!! voor alle mensen helpen met natuurkunde
U bent geweldig meneer Wietsma door U heb ik een 9.5 op mijn NASK toets bedankt. U bent een held.
Gefeliciteerd! En ik heb alleen maar geholpen, je hebt het zelf gedaan!
Kun u vraag 3 uitleggen?
Sorry voor het wat late antwoord
Je wilt weten welke stoffen bij 350 graden Celsius gas zijn, dan moeten ze dus al voorbij het kookpunt zijn. In de tabel kun je zien dat dit de volgende stoffen zijn:
Water, Alcohol, Stokstof en Olijfolie
Meneer is stokdtof niet stikstof????????
Helemaal gelijk, stikstof*
U bent geweldig meneer Wietsma door U heb ik een 9.9 op mijn toets bedankt.
Super, gefeliciteerd, maar de credits zijn voor jou! Jij hebt de toets gemaakt, ik heb slechts een beetje geholpen 😉
Dag meneer Wietsma,
Ik heb binnenkort een NaSk (natuurkunde/scheikunde) toets. Daar heb ik nog een vraag over. Ik moet namelijk weten hoe de moleculen van een stof zich gedragen als ze warmer worden. Weet u dat misschien?
Groetjes!
Zeker! Ze gaan trillen en harder bewegen!
Dat leg ik verder uit in deze twee video’s
https://meneerwietsma.nl/warmte/warmte-transport/
https://meneerwietsma.nl/stoffen/faseovergangen-en-kooktraject/ (tot 2:45)
Heeft u begrippen met betekenis op uw website ? zoals fase overgang meetbereik moleculen etc.
Helaas heb ik geen begrippenlijst beschikbaar.
dank u wel voor een top kanaal en website
U bent mijn redder in nood. Heb allemaal tentamens moest ze kennen voordat me vriendin mocht komen. ik kon het na wat aantekkeningen helemaal perfect topper
kunt u vraag 1 en 2 uitleggen ik snap er niks van en komende woensdag heb ik de toets
Bij vraag 1 is het 20 °C en je wilt weten welke stoffen vloeibaar zijn. Dat zijn de stoffen waarbij 20 °C tussen het smeltpunt en het kookpunt inzit. Dus: Water, alcohol, kwik en olijfolie.
Bij vraag 2 is het -1 °C en je wilt weten welke stoffen vast zijn. Dat zijn de stoffen waarbij -1 °C onder het smeltpunt zit (dan zijn ze nog niet gesmolten). Dus: water, ijzer, waxine.
Succes met de toets!
Beste mnr,
Uw videos zijn echt lifesavers!
Zou u ooit is een video kunnen maken over de fysica achter een Moka pot ( espressokannetje)?
( zijn werking uitleggen met behulp van de gaswetten,…)
Dankuwel
MVG
Fijn dat mijn video’s helpen!
De Moka pot is wel een heel erg klein onderwerp om een video over te maken. Over de gaswetten heb ik al wel video’s!